福建高考卷、化学试卷、2024年高考真题,教育小助手通过百度云盘、腾讯云盘分享Word版资源文件:2024年福建高考卷(化学)真题,若想获取Word版资源,请点立即下载!更多试题详解、参考答案、解析应有尽有,并且有海量历来真题,家长想要孩子提优就来下载打印刷真题吧
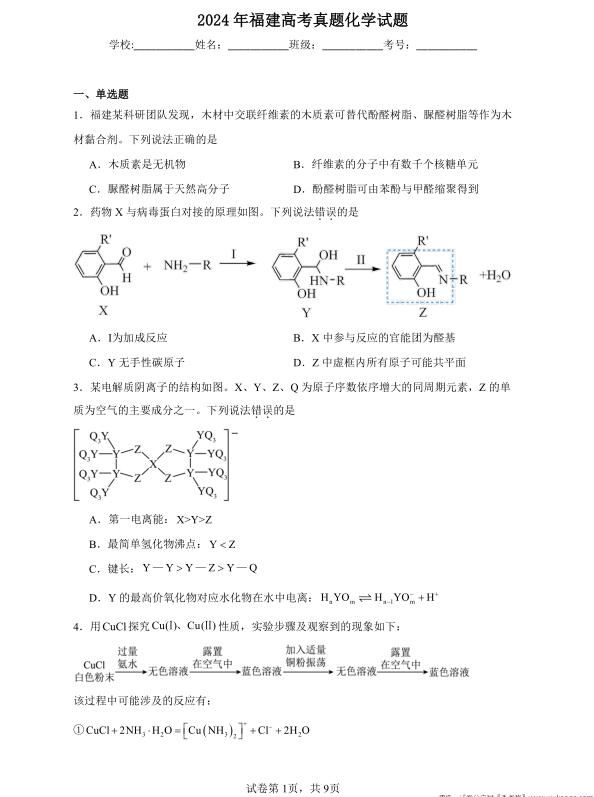

【详解】A.木质素为纤维素,属于多糖类,为有机物,A错误: B.纤维素的分子中有数千个葡萄糖单元,B错误: C.脲醛树脂由尿素和甲醛缩聚而成,属于合成高分子,C错误: D.酚醛树脂可由苯酚与甲醛缩聚得到,D正确: 故选D 2.C 【详解】A.对比X、Y的结构简式可知,X中醛基与HN-R中氨基发生加成反应,故A 正确: B.由以上分析可知X中参与反应的官能团为醛基,故B正确: C.由Y的结构简式可知,羟基所连碳原子为手性碳原子,故C错误: D.苯环为平面结构,C=N双键也为平面结构,因此虚框中所有原子可能共面,故D正确: 故选:C。 3.A 【分析】由该阴离子结构可知Z形成2条共价键,Z的单质为空气的主要成分之一,可知Z 为O:Y形成4条共价键,Y为C,Q形成1条共价键,Q为F,X得1个电子后形成4条 共价键,则X最外层电子数为3,X为B,据此分析解答。 【详解】A.B、C、O为同周期元素,从左到右,第一电离能呈增大趋势,则第一电离能: B<C<O,故A错误: B.CH4不能形成分子间氢键,HO可以形成分子间氢键,沸点CH4<HO,故B正确: C.原子半径:C>O>F,原子半径越小键长越短,则键长:C-C>C-O>C-F,故C正确: D.Y为C,其最高价氧化物的水化物为HCO3,碳酸为二元弱酸,分步电离,电离方程式 为:HCO=HCO+H,故D正确: 故选A。 4.A 【分析】CuCI加入过量氨水生成无色溶液,过程中发生反应 CuCI+2NH,H0=[CuNH,)2]+CI+2H,0,其中Cu(NH,)2(aq)为无色,无色溶 液在空气中被氧气氧化为蓝色溶液,发生反应 4[Cu(NH,2了+O,+8NHH,0=4[Cu(NH)]+4OH+6H,0,其中[Cu(NH)](aq) 为蓝色,加入铜粉发生反应[Cu(NH),]广+Cu=2[Cu(NH,了,放置在空气中又发生反应 4[Cu(NH2丁+O,+8NHH,0=4[Cu(NH)4]+4OH+6H,0,溶液又变为蓝色,据此 解答。 【详解】A.NH中由N原子提供孤对电子用于形成配位键,OH中由O原子提供孤对电 子用于形成配位键,电负性O>N,则O给电子能力弱,则与Cu+的配位能力:NH,>OH, 故A错误: B.由分析可知,[Cu(NH)2](aq无色,故B正确: C. 氧化剂的氧化性大于氧化产物,由方程式[Cu(NH)4]+Cu=2[Cu(NH)2了可知,氧 化性:[Cu(NH,)2]<[Cu(NH)4],故C正确: D,由分析可知,探究整个过程未发生反应②,故D正确: 故选A。 5.C 【分析】废线路板先机械粉碎,可以增加其反应的接触面积,加入稀盐酸后铝、锌、铁溶解, 进入滤液,通入氧气和加氢氧化钠,可以溶解锡和铅,最后电解精炼得到铜 【详解】A。机域粉碎的目的是增大接触面积,加快反应速率,A错误: B.酸溶的过程中Al、Zn、Fe转化为对应的A、Fe2和Zn2+离子,B错误: C.“碱溶时根据产物中SnO,存在反应:Sn+2OH+O,=SnO片+H,0,故C正确: D.电解精炼时粗钥在阳极发生氧化反应,逐步溶解,故D错误: 故远C。 6.B 【详解】A,1个N分子中有8个g键,每个o键含有2个电子,共16个电子,1.0moN,的 c键电子数为16N、,A正确: B.N分子中所有原子共面可知兰 1个N,分子1-6处的6个N原 子采取sp2杂化,7、8两处N原子采取s即杂化,其中8、1、3、4、5、6六处N原子各有 一对孤电子对即1个N。分子有6对孤电子对,1.0moN,的(价层)孤电子对数为6N。,B辑 误: C.N,分子中所有原子共面可知三N ,1个N.分子有6个N原子采取 sp2杂化,1.0molN的sp2杂化N原子数为6N,C正确: D.112.0gN,为112gmo 112g =lmol,含有8molN,根据氮原子守恒,1olN,完全分解产生4mol N2,D正确: 故答案为:B 7.B 【详解】A,己知电负性C>Br,因此氯在化合物中更容易吸引电子,导致I-CI比I-Br更 容易新裂,所以电高程度1C>IB,K<6.0×10,A正确: B.每个碘离子可以与一个碘分子结合,形成I:,这个过程中,高子能够离解成碘和琪离 子,形成平衡反应:+I=I,所以溶液中存在(q)己I(q)+厂(胸)的电离平衡,此 变化不是氧化还原反应,IC、ICI中琪元素是+I价,氯元素是-I价,Br和Br中,碘元 素是+1价,溴元素是-1价:三个变化过程中,各元素化合价都没有改变,不是氧化还原反 应,B错误: C,同主族元素从上往下,电负性逐渐减小,因此氮的电负性大于溴的电负性,形成共价键 的两元素之间的电负性的差值越大,则键的极性越强,因此共价键极性的大小关系为C>B, C正确: D.已知电负性C>Br,因此氯在化合物中更容易吸引电子,导致B-CI容易断裂产生为 BrCl(aq)和CI(aq),D正确: 故答案迹B。 8.C 【详解】A.DMF即N,N二甲基甲酰胺,对人体有危害,反应须在通风棚中进行,故A 正确: B.减压蒸馏利用沸点不同,去除CHOH、5-氧代己酸甲酯和DMF,可以提纯中间产物, 故B正确: C.减压蒸馏后不能趁热加入盐酸,因为盐酸具有挥发性,故C错误: D,1,3-环己二酮不含有亲水基团,不溶于水,可用少量冰水洗涤产物,除去盐酸等物质, 故D正确: 故选C。 9.D 【分析】放电过程中产生(C℉SO,),NLi,由图可知,放电过程中氯气得到电子发生还原反 应生成LiN,LiN又转化为(CFSO,),NLi和LiCI,则左侧电极为正极,右侧电极为负极: 【详解】A.放电过程中负极锂失去电子形成锂离子,锂离子通过阳离子交换膜进入左侧生 成(CFSO2)2NLi,A错误: B,鲤为活泼金属,会和水反应,故电解质溶液不能为水溶液,B错误: C.充电过程中电解LiC1失去电子发生氧化反应产生Cl2:2CT-2eCl,个,锂离子在阴极 得到电子发生还原生成卸单质:2Li+2e=2Li,则理论上每生成1 molCl2·同时生成2 molLi, C错误: D.由分析,放电过程中,正极氮气得到电子发生还原反应生成LN,LN又转化为 (CF,SO:),NLi和LiC1,负极锂失去电子发生氧化反应生成锂离子,总反应为 6Li+N2+4CESO,CI=2(CFSO2),NLi+4LiC1,D正确: 故选D. 10.D 【分析】草酸钙为强碱弱酸盐,其溶液呈碱性,滴加盐酸过程中体系中存在一系列平衡 CaC,0,(s)Ca(aq)+C,O(aq)、C,O+H,0HC,0+0H、 HC,O+H,OH,C,O,+OH,因此曲线I代表C,O:,曲线Ⅱ代表HC,O:,曲线I代表
样本阅读结束,请到下载地址中:阅读全文及下载