高三、2025年化学试卷、浙江省金华十校高三4月模考,教学小助手分享Word版资源文件:化学试卷-浙江省金华十校2025届高三4月模考,若想获取Word版资源,请点立即下载!更多试题详解、参考答案、解析应有尽有,并且有海量历来真题,提优就来下载打印刷真题吧!

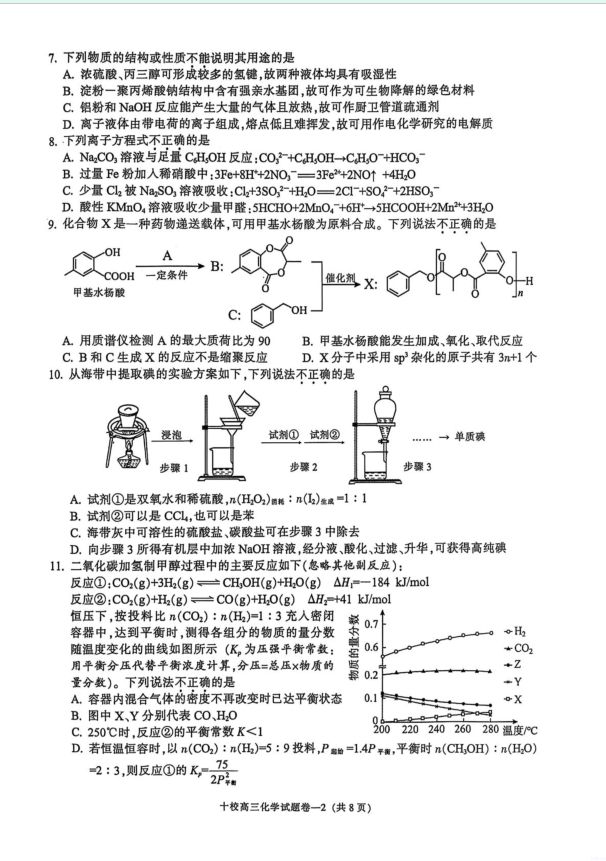
下列物质的结构或性质不能说明其用途的是 A.浓硫酸、丙三醇可形成较多的氢键,故两种液体均具有吸湿性 B.淀粉一聚丙烯酸钠结构中含有强亲水基团,故可作为可生物降解的绿色材料 C.铝粉和NaOH反应能产生大量的气体且放热,故可作厨卫管道疏通剂 D.离子液体由带电荷的离子组成,熔点低且难挥发,故可用作电化学研究的电解质 ·下列离子方程式不正确的是 A.NaCO溶液与足量CH,OH反应:CO,+CH,OH→CH,0+HCO B.过量Fe粉加人稀硝酸中:3Fe+8H'+2NO,ˉ一3Fe+2NO↑+4H,0 C.少量Cl2被NaS0,溶液吸收:C1+3S0,2+H0一2C1+S02+2HS0,ˉ D.酸性MnO4溶液吸收少量甲醛:5HCH0+2M血O,+6→5HC00H+2Mm+3Hz0 化合物X是一种药物递送截体,可用甲基水杨酸为原料合成。下列说法不正确的是 OH COOH一定条件 甲基水杨酸 A用质谱仪检测A的最大质荷比为90 B.甲基水杨酸能发生加成、氧化、取代反应 C.B和C生成X的反应不是缩聚反应 D.X分子中采用s即杂化的原子共有3n+1个 从海带中提取碘的实验方案如下,下列说法不正确的是 泡 试剂①试剂② ……→单质碘 步骤1 步骤2 步骤3 A试剂①是双氧水和稀硫酸,n(H0)耗:n()成■1:1 B.试剂②可以是CCL,也可以是苯 C.海带灰中可溶性的硫酸盐、碳酸盐可在步骤3中除去 D.向步骤3所得有机层中加浓NOH溶液,经分液、酸化、过滤、升华,可获得高纯碘 二氧化碳加氢制甲醇过程中的主要反应如下(忽略其他副反应): 反应①:C02(g)+3H(g)CH0H(g)+H0(g) △H=-184kJ/mol 反应②:C0(g)+H(g)=C0(g)+H0(g)△H2+41 kJ/mol 恒压下,按投料比n(CO):n(H)=1:3充人密闭 兹0.7 容器中,达到平衡时,测得各组分的物质的量分数 0000 H2 随温度变化的曲线如图所示(K,为压强平衡常数: 0.6 +C02 用平街分压代替平衡浓度计算,分压=总压×物质的 +Z 量分数)。下列说法不正确的是 0.2 Y A.容器内混合气体的密度不再改变时已达平衡状态 0.1 oX B.图中X、Y分别代表C0、HO 0.2.90i0-9 C.250℃时,反应②的平衡常数K<1 200220240260 280温度/℃ D.若恒温恒容时,以n(C02):n(H)-5:9投料,P=4P南,平衡时n(CHOH):n(H,O) 2:3,则反应①的K75 冰晶石(QN,AF)的品胞结构如下图所示。下列说法正确的是 A.Na AIF。品体属于混合型品体 B.与浓硫酸共热,可产生亚气体 C.C1原子的3p能级给出电子对能力比F原子的2p能级弱,故不 存在Na,A1Cl D.NaAF6晶体中,A1原子中的2d、3s、3p等轨道进行杂化形成6 个杂化轨道 已知:将工业废气(主要成分CO2和SO2)通人足量NaHCO,溶液获得溶液A和CO2,如下 装置可实现污染治理和C0、S0的综合利用。下列说法不正确的是 溶液A C02 SO,+H,O CO: 0H,0 H,SO 质子交换膜 so HCOOH 电极1 电极2 电极3 电极4 装置① 离子交换膜 装置② A.装置①实现了化学能转化为电能 B.电极2发生的反应为:0+4e+4H=2H0 C.反应一段时间后,装置②的阳极区溶液pH降低 D.治理过程中参与反应的SO2、C02物质的量之比为1:1 化合物X在H催化下可转化为M和少量其它烯烃副产物。下列说法不正确的是A.步骤①,量取卤代烃时可用碱式滴定管 B.步骤①,卤代烃发生消去反应不会影响卤素百分含量的测定 C.步骤③,若得到的固体呈黄色,则卤代烃中含碘元素 D.步骤③,先水洗再乙醇洗,可使卤素百分含量测定结果更准确 非选择题部分 二、非选择题(本大题共4小题,共52分) 17.(16分)氮是自然界中普遍存在的元素,也是生命活动中不可或缺的元素。 请回答: (1)关于氮元素相关的结构与性质,下列说法正确的是▲ A.基态N原子的电子排布式可表示为1s2s2p.2py2p. B.液氨中存在2NH→NH+NH2ˉ,NH2中N的杂化方式为p2 C.将NH通人H0中,形成的氢键强弱:O一H·N>N一HO D.NHOH中的H一N一O键角比H,OH中的H一N一O键角大 (2)某化合物A的晶胞如图。 ①化学式是▲一; ②将2.28g该化合物加人到盛有20mL水 的烧杯中,充分搅拌后可以观察到的现象 是▲。 (3)NH可以与多种金属离子形成配合物。已知: Co+具有强氧化性,[Co(NH)严性质稳定; 。NH Co不易被氧化,[Co(NH)+具有较强还 原性。 Fe ①请分析Co"和[Co(NH)*氧化性差异的
样本阅读结束,请到下载地址中:阅读全文及下载