江苏省镇江市2024-2025学年高三下学期期初质量监测,高中\高三\江苏省\2024-2025学年下\江苏省镇江市丹阳市\化学三零论坛(30论坛)用百度云盘、腾讯云盘分享的原卷版、解析版及答案,在云盘中的课件资料可在线阅读及保存到自己的云盘,此电子版课件永久免费阅读及下载。

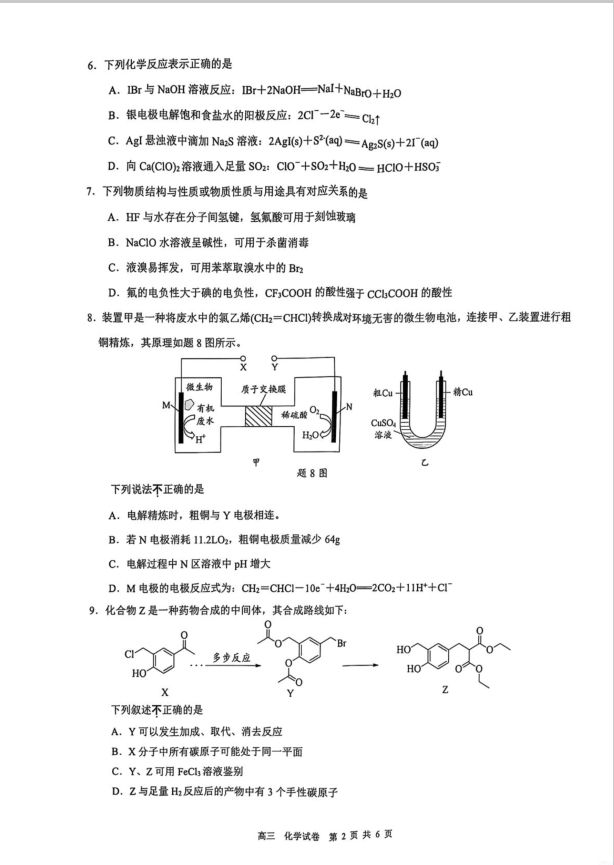
镇江市20242025学年度第二学期高三期初质量监测 化学答案 2025.02 一、选择题(共13题,每题3分,共39分) 2 3 4 5 6 7 8 9 10 B A C A C C D B A D 11 12 13 c B D 二、非选择题(共4题,共61分) 14.(1)①Fe 3d> 4分 ②过高的F+会水解生成氢氧化铁覆盖在铁酸锌表面,不利于铁酸锌溶解。 2分 3ZnFe204+2H2S04+SO:=ZnS04+2FeS0.+2H:O 3分 (2)①由于HO,与Fe的电极电势相差不大,还原速率慢:H:O:与MnO2的电极电势差 较大,还原速率快,所以铁浸出率远低于锰 3分 ②柠檬酸既有酸性又有强还原性,自身能还原LC0O,中的三价钻 2分 【共14分】 15.(1)吸收反应生成的HC1,提高B的产率。 2分 (2)醚键、酯基 2分 (3) 3分 COOCH (4) HCOO OOCH 3分 COOH 5 KMnO/1I (C0C)2 AlCl.DCM OH KBH HBr CHOH i-PrOH 5分 【共15分】 16.(1)N2H4-H:0+2MnO2=N2+2MnO+3H20 2分 (2)①0C ONH4 或 0-C<OH·NH 2分 NHz NH O-Mn-ONH, ②温度超过50C时,0=C 受热分解生成碳酸锰沉淀,故锰的浸取率迅速下 NH, 6.下列化学反应表示正确的是 A.Br与NaOH溶液反应:Br十2NaOH一Nal十NaBrO+HO B.银电极电解饱和食盐水的阳极反应:2C一2c=Ct C.AgI悬浊液中滴加NaS溶液:2AgI(S)十S(aq=AgS(9)+2(aq D.向Ca(ClO溶液通入足量S02:Cl0+SO2十H0==HC10+HS0j 7.下列物质结构与性质或物质性质与用途具有对应关系的是 A,亚与水存在分子间氢键,氢氯酸可用于刻蚀玻璃 B.NaClo水溶液呈碱性,可用于杀菌消毒 C.液溴易挥发,可用苯萃取溴水中的B2 D.氟的电负性大于碘的电负性,CF3COOH的酸性强于CCbCOoH的酸性 8.装置甲是一种将废水中的氯乙烯(CH2=CHC)转换成对环境无害的微生物电池,连接甲、乙装置进行粗 铜精炼,其原理如题8图所示。 微生物 质子交换展 有机 CuSO H.o 溶液 题8图 下列说法不正确的是 A.电解精炼时,粗酮与Y电极相连。 B.若N电极消耗11.2L02,粗铜电极质量减少64g C.电解过程中N区溶液中pH增大 D.M电极的电极反应式为:CH2=CHC一10e+4H0-2C02+11H+C1 9。化合物Z是一种药物合成的中间体,其合成路线如下: 多步反应 HO X 下列叙述不正确的是 A.Y可以发生加成、取代、消去反应 B.X分子中所有碳原子可能处于同一平面 C.Y、Z可用FeCl,溶液鉴别 D,Z与足量H反应后的产物中有3个手性碳原子 10.下列所给物质在给定条件下能实现一步转化的是 A.FeS0 HsO B.饱和NaC溶液道电Na Tick()Ti 高温 C.NHy(g) △化肃N0g)0mNOo 0z(8) D.Fe203- Co→FeH,O8Fe,04 高温 高温 11,室温下,根据下列实验过程及现象,能验证相应实验结论的是 选项 实验方案 实验结论 向2mL浓度均为0.1 mol-LNa2C0,和Na2S0:的混合溶液中滴加几 滴0.1molL-BaCl溶液,有白色沉淀产生 Kip(BaS04)<K(BaCO3) 将FeO4溶于盐酸所得溶液浓缩后,滴入酸性KM如O4溶液,酸性 B KMnO:溶液褪色 FeO4中含有Fe) c 相同条件下,用30mL1.0 nol-LCHC00H溶液和40mL1.0moL 盐酸分别做导电性实验,醋酸溶液对应的灯泡较暗 CH:COOH是弱电解质 D 用pH计分别测定NaCIO和NaAIO2溶液的pH,前者pH大 结合H的能力: AlO2>CIO 12.室温下,HP04是一种中强酸(KHP0)=7.1×103,KHP0)=6.3×10,K(HP0)=4.2×10), 下列说法正确的是 A,溶液pH=4时:cHPO):c阳PO)=0.71 B.0.1moL的NazHP04溶液中:c(H2PO4)+2cHP0)>cPOi) C.向0.1 nol/LNaH2P04溶液中加入足量Ca(OHD2:HPoi+2OH一P01+2H0 D.(NaH2PO4):NazHPO4)=1:1的混合溶液中: 3c(Na*)=2[c(H3PO4)+c(H2PO)+c(HPO)+c(PO ) 13.C02的捕集与转化是“碳达峰•碳中和"的有效途径。利用CH4和C02制备合成气C0和H2的原理如下: ①CH4(g)+C0z(g)=2H(g)+2C0(g)△H 100 山线甲+曲线乙 ②COz(g)十H(g)=CO(g)+HO(g)△H 80 在恒压为pkPa,起始时(CH:mCO)=1:1条件下,CH和COz的 60 c(800,40 平衡转化率与温度的关系如题13图所示。 401 下列说法不正确的是 20 A,随着温度升高,体系中HO(g)物质的量一直增大 b(800,20 B.反应CH4(g)+2C0(g)=H(g+3C0(g+HO(g)的△H>0 600700800900100011001200 温度K C.800K时,反应开始经过1min达到平衡状态,C0的体积分数为25% 题13图 D.在反应器中充入CH,和C02制备合成气,增大压强能提高合成气平衡产率
样本阅读结束,请到下载地址中:阅读全文及下载